Preparatomtale
C ▼Legemiddelet er under særlig overvåkning
Xembify® 200 mg/ml injeksjonsvæske, oppløsning
Indikasjoner: Substitusjonsbehandling hos voksne, barn og ungdom (0–18 år) ved:
- Primære immunsviktsykdommer (PID) med nedsatt antistoffproduksjon.
- Hypogammaglobulinemi og tilbakevendende bakterieinfeksjoner hos pasienter med kronisk lymfatisk leukemi (KLL), hvor profylaktiske antibiotika ikke har virket eller er kontraindisert.
- Hypogammaglobulinemi og tilbakevendende bakterieinfeksjoner hos pasienter med myelomatose.
- Hypogammaglobulinemi hos pasienter før og etter allogen hematopoetisk stamcelletransplantasjon. (HSCT)
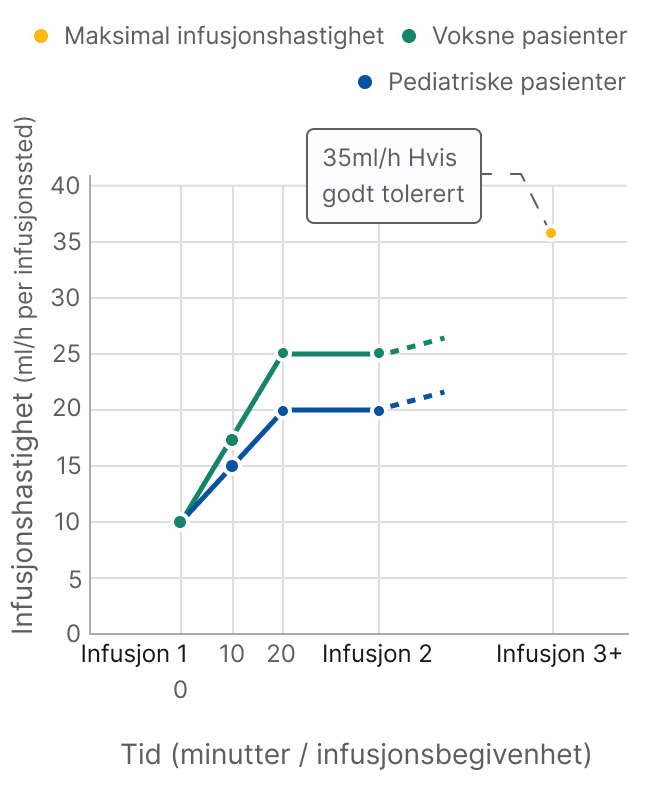
Dosering: Substitusjonsbehandling skal startes og overvåkes under tilsyn av lege med erfaring i behandling av immunsvikt. Dosen tilpasses individuelt, avhengig av farmakokinetisk og klinisk respons. Dose basert på kroppsvekt kan kreve justering hos pasienter som er under- eller overvektige. Doseregimet bør gi bunnkonsentrasjon av IgG (målt før neste infusjon) ≥5-6 g/liter og ha som mål å ligge innenfor referanseintervallet for serum-IgG iht. alder. Metningsdose på ≥0,2-0,5 g/kg (1-2,5 ml/kg) kroppsvekt kan være nødvendig, og må kanskje fordeles over flere dager, med maks. daglig dose 0,1-0,15 g/kg. Når steady state IgG er nådd, gis vedlikeholdsdoser med gjentatte intervaller for å oppnå samlet månedlig dose på 0,4-0,8 g/kg. Administrering: Kun til s.c. bruk, infusjonsstedet skal roteres. Justering av infusjonshastighet/-volum pr. sted, baseres på pasientens toleranseevne.
Kontraindikasjoner: Overfølsomhet for innholdsstoffene eller humant immunglobulin. Alvorlig IgA-mangel. Skal ikke gis i.v. eller i.m.
Advarsler og Forsiktighetsregler: Sporbarhet: For å forbedre sporbarheten til biologiske legemidler, skal navn og og batchnummer til det administrerte legemiddelet journalføres. Utilsiktet administrering i blodåre kan gi sjokk. Anbefalt infusjonshastighet og administrerings- instruksjoner skal følges nøye. Pasienten skal overvåkes nøye for ev. tegn til bivirkninger i infusjonsperioden (første gangs behandling i 1 time, andre i minst 20 min.). Ved bivirkninger skal administreringshastigheten reduseres eller infusjonen stoppes. Pasienter med anti-IgA-antistoffer har økt risiko for allergiske reaksjoner, og skal kun behandles under tilsyn der behandling med s.c. IgG-preparater er eneste alternativ. Forsiktighet skal utvises ved risikofaktorer for tromboemboliske hendelser. Pasienten skal være tilstrekkelig hydrert før administrering. Pasienter med nedsatt nyrefunksjon skal overvåkes. Aseptisk meningittsyndrom (AMS) er sett. Ved bivirkninger bør bilkjøring og bruk av maskiner unngås inntil de går over.
Interaksjoner: Vaksiner med levende, svekkede virus skal ikke gis de første 3 månedene etter behandling, da immunglobuliner kan redusere effekten av vaksiner. For meslinger kan redusert effekt vedvare i opptil 1 år.
Bivirkninger: Svært vanlige (≥1/10): Generelle: Lokal reaksjon på infusjonsstedet. Vanlige (≥1/100 til <1/10): Gastrointestinale: Diaré, kvalme. Generelle: Feber. Hud: Papel, pruritus. Infeksiøse: Rhinitt. Muskel-skjelettsystemet: Artralgi, ryggsmerter. Nevrologiske: Hodepine. Undersøkelser: Redusert immunglobulin G i blod. Frekvens ikke kjent: Dyspné, fatigue.
Pakninger, priser og refusjon pr. 15.05.2024: Xembify® er med i anbudet «2422 Plasmaderiverte legemidler» med rabatterte priser. 5 ml (hettegl.): Varenr.: 189759. 1 082,30 Kr., 10 ml (hettegl.): Varenr.: 420945. 2 128,40 Kr., 20 ml (hettegl.): Varenr.: 160633. 4 220,50 Kr., 50 ml (hettegl.): Varenr.: 084561. 10 496,80 Kr. Refusjon H- resept /(reseptgr. C).
Seneste produktresume (SPC) godkjent av DMP: 2024-04-26. For fullstendig informasjon se Felleskatalogen: www.felleskatalogen.no
Grifols Nordic AB
Telegrafgatan 6, 169 72 Solna, Sweden | +46 (0)8 441 89 50 | www.grifols.com | infonordic@grifols.com